AI驱动从头设计多样化小分子结合蛋白,韩国团队发现能选择性识别压力激素的蛋白质
韩国科学技术院生物科学系联合美国华盛顿大学西雅图分校蛋白质设计研究所,依托人工智能技术,成功实现了蛋白质的“从头设计”,创建出可选择性识别应激激素皮质醇及其他小分子化合物的人造蛋白质。该研究成果已在《自然·通讯》杂志发表,标志着小分子结合蛋白设计领域的一大突破。
背景:小分子识别蛋白设计的长期挑战
- 蛋白质从头设计旨在根据功能需求生成全新的结构与序列,但长期以来面临原子层面精确控制与功能实现的双重难题。
- 小分子结合蛋白在医学和环境监测中至关重要,然而天然蛋白的结构多样性受限,传统方法多依赖筛选或局部改造,难以满足对特定目标的精准识别需求。
- 团队聚焦于NTF2蛋白家族,尝试通过人工智能手段构建具有多样化结合口袋但结构仍保持模块化的设计框架。
技术路径:多AI模型协同设计,实现精准功能构建
研究人员采用多个AI模型协同工作,构建出具备高精度的小分子结合蛋白设计体系:
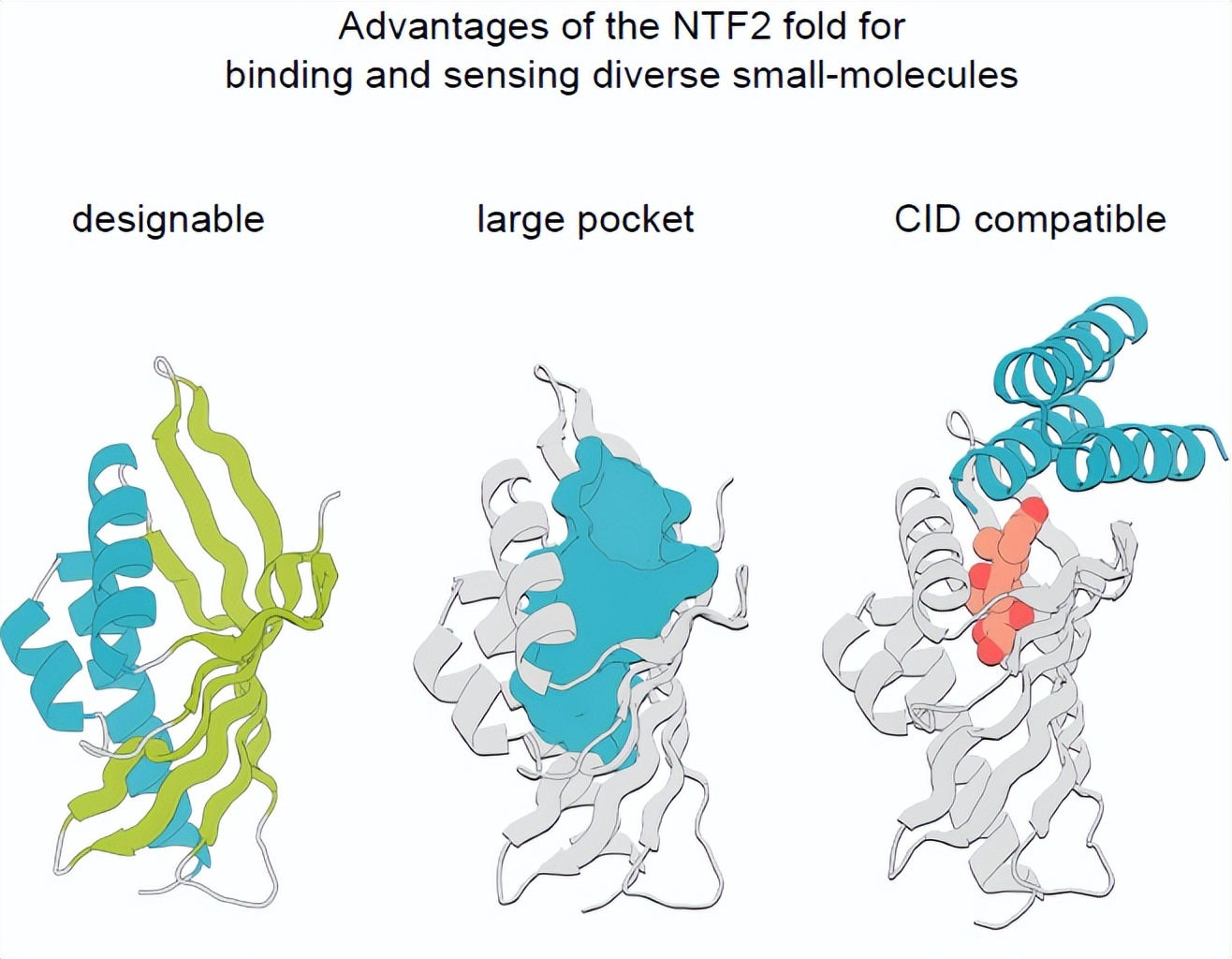
- RIFdock:用于将小分子配体精准嵌入到NTF2结构骨架的中心口袋。
- LigandMPNN:基于蛋白-小分子复合物数据训练的AI模型,专门用于在序列设计过程中显式考虑配体存在。
- ProteinMPNN:用于提高蛋白结晶性,实现表面重设计,优化结构与功能的一致性。
- Rosetta:作为辅助工具,用于计算筛选和结构优化。
设计过程中,研究人员共生成超过10,000个NTF2骨架,并将六种化学性质与结构各异的小分子嵌入其中,包括:
- 应激激素皮质醇(HCY)
- 抗凝药华法林(WRF)
- 肌肉松弛剂罗库溴铵(ROC)
- 抗凝药阿哌沙班(APX)
- 抗癌药活性分子SN-38(IRI)
- 激素17-α-羟基孕酮(OHP)
实验验证:高分辨率结构确认AI设计准确性
为验证设计成果,研究团队解析了两种蛋白-配体复合物的晶体结构:
- 皮质醇结合蛋白 hcy129:通过ProteinMPNN进行表面重设计后,获得高分辨率(1.5 Å)结构,整体折叠与设计模型高度一致(Cα RMSD 为 1.1 Å)。
- 阿哌沙班结合蛋白 apx1049:同样显示出与预测模型匹配的结构特征,验证了氢键网络(HBNet)在极性相互作用设计中的有效性。
此外,团队进一步设计了皮质醇依赖的异源二聚体系,引入小型蛋白骨架 miniH11,最终成功构建出一个可与 hcy129.1 及皮质醇形成三元复合物的系统,为生物传感器开发奠定了结构基础。
研究影响:开启精准生物传感与定制化蛋白设计新纪元
- 疾病早筛:未来可实现血液中生物标志物的痕量检测,推动疾病早期诊断技术发展。
- 新药研发:通过定向设计小分子识别蛋白,为靶向药物筛选和开发提供高效工具。
- 环境监测:定制化生物传感器有望应用于空气和水质中微量污染物的实时监测,推动生态健康治理技术进步。
- 标准化流程:研究团队建立的AI结合生物物理法则的设计流程,被学界认可为新型标准,具有广泛推广价值。
前景展望:AI在蛋白质设计中的深度整合
这项研究展示了AI在从头蛋白质设计中的强大能力,未来有望进一步融合量子力学等多学科方法,提升设计精度和应用广度。AI不仅能够“预测”结构,更可以“生成”功能,为构建全新生命系统提供坚实基础。
